เป็นที่ทราบกันดีว่า COVID-19 เป็นโรคที่เกี่ยวข้องกับการติดเชื้อในระบบทางเดินหายใจแบบเฉียบพลัน แต่ไม่เพียงแค่ระบบทางเดินหายใจเท่านั้น โควิดยังมีความสัมพันธ์กับระบบทางเดินอาหารด้วย โดยผ่านทางการเปลี่ยนแปลงของจุลินทรีย์ในลำไส้ แล้วมันเกี่ยวกันอย่างไร?
จุลินทรีย์ในลำไส้นอกจากจะมีบทบาทในการส่งเสริมระบบภูมิคุ้มกันของร่างกายแล้ว ยังมีความเกี่ยวข้องกับความไวในการติดเชื้อไวรัสที่ปอดด้วย ในขณะเดียวกันการติดเชื้อไวรัสที่ปอดก็ส่งผลต่อองค์ประกอบของจุลินทรีย์ในลำไส้[1] เชื้อโควิดหรือ SARS-CoV-2 นอกจากจะสามารถพบได้ทั้งที่โพรงจมูกแล้วยังพบได้ในระบบทางเดินอาหาร และอุจจาระ ของผู้ป่วยโควิดด้วย [2] ทั้งนี้เนื่องจากเชื้อดังกล่าว เมื่อเข้าสู่ร่างกาย จะไปเกาะกับตัวรับที่ชื่อ ACE2 ซึ่งมีอยู่ในหลายๆ อวัยวะ รวมถึงระบบทางเดินหายใจและทางเดินอาหาร [3] การที่เชื้อไปจับกับตัวรับดังกล่าวทำให้การทำงานของตัวรับนั้นบกพร่องไป ส่งผลให้เกิดการเสียสมดุลของระบบภูมิคุมกันและการเกิดภาวะเสียสมดุลของจุลินทรีย์ในลำไส้ (Dysbiosis) [4] มีงานวิจัยพบว่า ผู้ป่วยโควิดมีการลดลงของจุลินทรีย์ตัวดีในลำไส้ลดลง เช่น Lactobacillus และ Bifidobacterium [5] ผลที่ตามมาคือร่างกายจะติดเชื้อหรือถูกโจมตีจากจุลินทรีย์ก่อโรคได้มากขึ้น และมีการเพิ่มขึ้นของจุลินทรีย์ก่อโรคในลำไส้ ส่งผลต่อการตอบสนองทางภูมิคุ้มกันในภาวะโควิด เช่น ทำให้เกิดการหลั่งสารที่ทำให้เกิดการอักเสบ (proinflammatory cytokines) เช่น IFN-γ และ TNF-α [1] อีกรายงานหนึ่งพบว่าจุลินทรีย์ก่อโรคในลำไส้ เช่น Escherichia coli และ Klebsiella pneumoniae มีจำนวนเพิ่มขึ้นในผู้ป่วยโควิดในภาวะวิกฤต และยังมีความสัมพันธ์เชิงบวกกับความรุนแรงของโรคและโอกาสในการเสียชีวิตด้วย นี่เป็นประเด็นที่น่าสนใจ [6]
โพรไบโอติกส์ คือจุลินทรีย์ที่มีชีวิตซึ่งมีประโยชน์ต่อสุขภาพเมื่อรับประทานในปริมาณที่เพียงพอ [7]. จุลินทรีย์เหล่านี้ก็เป็นกลุ่มเดียวกับจุลินทรีย์ตัวดีที่อาศัยอยู่ในลำไส้ของมนุษย์เรานั่นเอง ด้วยสมบัติในการต้านจุลินทรีย์ก่อโรค เสริมสร้างระบบภูมิคุ้มกันและช่วยปรับสมดุลของจุลินทรีย์ในลำไส้ โพรไบโอติกส์จึงเป็นที่สนใจในการนำมาเป็นโภชนาการเสริมในผู้ป่วยโควิด เพื่อปรับให้จุลินทรีย์ในลำไส้ให้เกิดความสมดุล ทั้งนี้มีการศึกษาทางคลินิกพบว่าการทานโพรไบโอติกส์บางชนิดช่วยป้องกันการติดเชื้อจากแบคทีเรียและไวรัสในระบบทางเดินหายใจได้ และการใช้ในผู้ป่วยวิกฤติยังพบว่าช่วยลดโอกาสของการเกิดปอดอักเสบที่เกี่ยวข้องกับเครื่องช่วยหายใจ (ventilator-associated pneumonia) ด้วย อย่างไรก็ตามยังไม่มีงานวิจัยที่รายงานเรื่องผลของการให้โพรไบโอติกส์ในผู้ป่วยโควิด ต้องติดตามกันต่อไป แต่ถ้าเราอยากเสริมภูมิต้านทานให้กับร่างกายไว้เตรียมพร้อมรับมือต่อโรคภัย การรับประทานอาหารที่โพรไบโอติกส์เป็นประจำก็เป็นอีกทางหนึ่ง
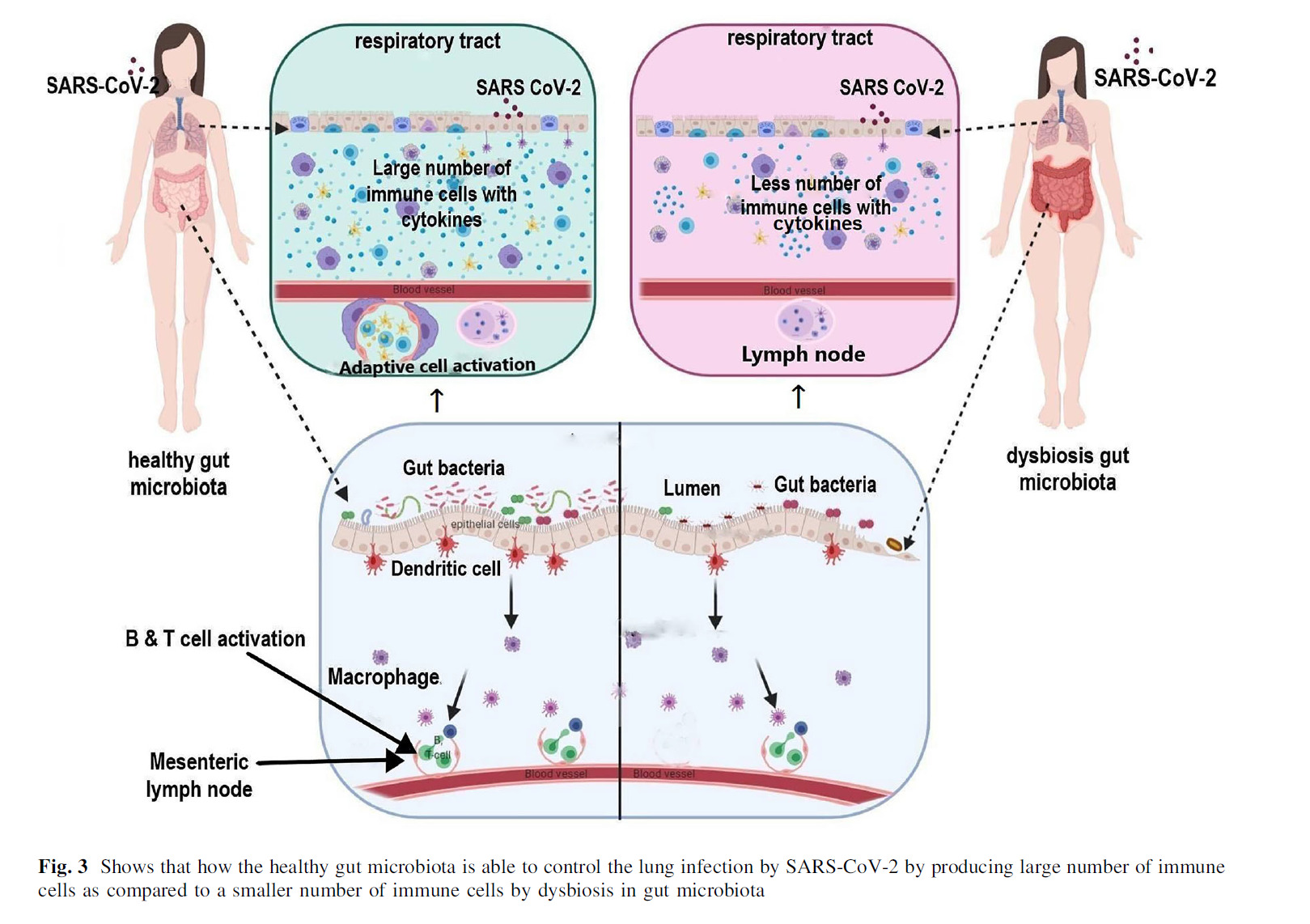
รูปภาพ แสดงกลไกของจุลินทรีย์ในลำไส้ที่อยู่ในภาวะสมดุล (healthy gut microbiota) ในการควบคุมการติดเชื้อ SARS-CoV-2 โดยการผลิตเซลล์ภูมิคุ้มกันเป็นจำนวนมาก แต่หากจุลินทรีย์ในลำไส้เสียสมดุล (dysbiosis gut microbiota) จะผลิตเซลล์ภูมิคุ้มกันได้เพียงจำนวนน้อย [10]